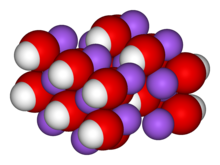
Hidroxid de sodiu
| Hidroxid de sodiu | |
 | |
| Denumiri | |
|---|---|
| Alte denumiri | leșie, sodă caustică |
| Identificare | |
SMILES [OH-].[Na+][1]  | |
| Număr CAS | 1310-73-2 |
| ChEMBL | CHEMBL2105794 |
| PubChem CID | 14798 |
| Informații generale | |
| Formulă chimică | NaOH |
| Aspect | substanță solidă, de culoare albă |
| Masă molară | 39,997 g/mol |
| Proprietăți | |
| Densitate | 2,130 g/cm3 |
| Starea de agregare | solidă |
| Punct de topire | 322°C |
| Punct de fierbere | 1.388 °C |
| Solubilitate | ușor solubil în apă, 1260 g/l (20 °C) |
| Presiune de vapori | 13 Pa (618 °C) |
 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
Modifică date / text  | |
Hidroxidul de sodiu (denumit și sodă caustică sau leșie) este o bază anorganică cu formula chimică NaOH. Ca formă de agregare este un corp solid, higroscopic, de culoare albă, fiind format dintr-un cation de sodiu și un anion hidroxid.
Soda caustică este o substanță puternic alcalină și caustică (pH=14 la c=1 mol/l), iar prin contactul cu pielea cauzează arsuri chimice severe. Este foarte solubilă în apă și higroscopică, absorbind umiditatea și dioxidul de carbon din atmosferă. Formează diverși hidrați cu formula NaOH·nH
2O.[2]
Reacționează cu dioxidul de carbon din aer, rezultând carbonat de sodiu, din această cauză soda caustică se păstrează în vase închise ermetic, pentru a evita contactul cu aerul sau umezeala.
Hidroxidul de sodiu este utilizat în foarte multe procese industriale, câteva exemple fiind: fabricarea hârtiei, textilelor, săpunurilor și detergenților. În anul 2004, producția la nivel mondial a fost de aproximativ 60 milioane de tone, iar cererea a fost de 51 milioane de tone.[3]
Utilizări

- Hidroxidul de sodiu este folosit în cantități mari în multe industrii, mai ales ca solvent apos alături de hidroxidul de potasiu.
Este folosit pentru:
- Obținerea de celuloză și hârtie din lemn sau paie,
- Produse chimice și materiale plastice,
- Fabricarea de săpun și detergenți,
- Fabricarea coloranților,
- Sinteza unor fibre textile artificiale,
- Mercerizarea bumbacului (bumbacul devine mai mătăsos, ușor de colorat, mai rezistent
- Obținerea de aluminiu (prelucrarea bauxitei).

- Curățarea de ulei, grăsimi, petrol
- Rafinarea chimică a uleiului alimentar
- Sinteza chimică a diferitelor produse ca: hipoclorit de sodiu, fosfat de sodiu, sulfit de sodiu, aluminat de sodiu
- Sinteza de acid formic
- Producerea apei demineralizate: pentru a reglementa pH-ul și de a regenera schimbul de ioni staționari în rășini la tratarea apei.
- În electronică: producerea plăcilor conductoare (ca. 10g/l bei 20 °C)
- Este parte componentă a substanțelor de curățare a conductelor
- Proprietatea caustică e folosit în tratarea plăcilor de cupru pentru producătorii de modele
- Curățarea recipientelor din oțel sau metal inoxidabil
- Îndepărtarea coloranților
- În 1883 a fost fabricată o locomotivă cu aburi cu sodă fără folosirea focului
- În industria agro-alimentară se utilizează la curățarea instalațiilor (circuite, sticlă), modificarea amidonului, peeling chimic etc. Este, de asemenea, un aditiv alimentar (E524[4]), plus servește ca regulator de aciditate[5] și este utilizat într-o gamă largă de produse[6].
- Producția mondială în 1998 a fost de aprox. 45 de milioane de tone. Hidroxidul de sodiu este solventul cel mai frecvent utilizat în laborator.
- Soda poate fi folosită pentru stocarea energiei solare în formă chimică. Ca efect, reacția dintre sodiu și apă este puternic exotermă. Soda diluată încă o dată, este utilizată pentru energia solară doar pentru a evapora apa și a reveni la starea inițială.
- Soda mai este utilizată ca reactiv pentru teste chimice. Într-adevăr, în prezența anumitor cationi metalici, hidroxidul de sodiu se precipită într-o anumită culoare.
Proprietăți fizico-chimice
- Substanță leșioasă
- Puternic electrolit favorizând electroliza apei
- Se dizolvă în substanțele polare degajându-se căldură de diluare
- Neutralizează acizii formând sărurile corespunzătoare radicalului ns
- Reacționează cu clorul, producând hipoclorit de sodiu (soluție diluată și rece) sau clorat de sodiu (soluție fierbinte concentrată):
- la rece
- la cald
Producerea
- Prin substituție a carbonatului de sodiu cu hidroxid de calciu, rezultând hidroxid de sodiu și carbonat de calciu:
Carbonatul de calciu mai puțin solubil va fi separat prin filtrare, în soluție rămânând numai soda caustică.
- Prin electroliză din clorură de sodiu (NaCl) -> leșie(NaOH) și clor
- Procedeul industrial (de producere, purificare și concentrare a Na(OH) :
- Metoda amalgam
- Metoda diafragmei
- Metoda membranei
- În laborator se poate obține direct din sodiu și apă:
- După procesul de condensare se obține soda caustică:
Vezi și
Referințe
- ^ „Hidroxid de sodiu”, SODIUM HYDROXIDE (în engleză), PubChem, accesat în
- ^ P. R. Siemens, William F. Giauque (1969): "Entropies of the hydrates of sodium hydroxide. II. Low-temperature heat capacities and heats of fusion of NaOH·2H2O and NaOH·3.5H2O". Journal of Physical Chemistry, volume 73, issue 1, pages 149–157. doi:10.1021/j100721a024
- ^ Cetin Kurt, Jürgen Bittner (), „Sodium Hydroxide”, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a24_345.pub2
- ^ Parlamentul European și Consiliul Europei (). „Directiva 95/2/CE despre aditivii alimentari cât și despre coloranți și despre îndulcitori”. Jurnalul official al Uniunii Europene. pp. 1–56. 95/2/CE. Accesat în . Parametru necunoscut
|no=ignorat (ajutor). - ^ Codex alimentarius, ed. (). „Clasificarea și Sistemul de Numerotare Internațional pentru aditivi alimentari”. http://www.codexalimentarius.net. CAC/GL 361989. p. 1-35. Codex_Alimentarius. Arhivat din original la . Accesat în . Legătură externa în
|site=(ajutor). - ^ engleză {{{1}}} Comisia Codex Alimentarius (2008). „Updated up to the 31st Session of the Codex Alimentarius Commission for Sodium hydroxide (524)”. http://www.codexalimentarius.net. GSFA Online. Codex Alimentarius. codex-gfsa-256. Arhivat din original la 2015-09-23. Accesat în 3/10/2008.. Verificați datele pentru:
|access-date=(ajutor); Legătură externa în|site=(ajutor)
Legături externe
- Produse clorosodice Arhivat în , la Wayback Machine.
- Sodă caustică Arhivat în , la Wayback Machine.
| |||||

















