Idruro di alluminio
| Idruro di alluminio | |
|---|---|
 | |
| Nome IUPAC | |
| Triidruro di alluminio | |
| Nomi alternativi | |
| Idruro di alluminio, alano | |
| Caratteristiche generali | |
| Formula bruta o molecolare | AlH3 |
| Massa molecolare (u) | 29,99 |
| Aspetto | Solido cristallino bianco, non volatile, altamente polimerizzato. |
| Numero CAS | 7784-21-6 |
| Numero EINECS | 232-053-2 |
| PubChem | 14488 |
| SMILES | [AlH3] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1 486 |
| Solubilità in acqua | Reattivo |
| Temperatura di fusione | 150 °C |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
  | |
| Modifica dati su Wikidata · Manuale | |
L'idruro di alluminio è un composto chimico avente come formula AlH3. È un solido instabile sopra i 150 °C. Ha proprietà riducenti e reagisce violentemente con acqua e altre sostanze protiche liberando idrogeno. Non ha utilizzi pratici significativi, e non è disponibile in commercio.
Storia
AlH3 fu sintetizzato per la prima volta nel 1942 da Egon Wiberg (1901-1976).[1]
Struttura
L'idruro di alluminio è un solido polimerico. Sono possibili molti polimorfi, chiamati α-, β-, γ-, δ-, ε- e θ-AlH3. La forma α-AlH3 è la più stabile e ne è stata determinata la struttura tramite diffrazione dei raggi X e diffrazione neutronica. Ogni atomo di alluminio è circondato da sei atomi di idrogeno che fanno da ponte ad altri sei atomi di alluminio. Le distanze Al–H sono tutte equivalenti (172 pm) e l'angolo Al–H–Al è di 141°.[2]
 | 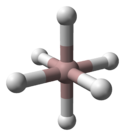 |  |
Cella primitiva di α-AlH3 | Coordinazione di Al | Coordinazione di H |
Sintesi
La sintesi più conveniente si effettua facendo reagire in soluzione eterea di tetraidroalluminato di litio LiAlH4 e tricloruro di alluminio AlCl3 in condizioni rigidamente controllate. A seconda delle condizioni usate si può determinare quale polimorfo ottenere:[3]
- 3LiAlH4 + AlCl3 + nEt3O → 4[AlH3(Et3O)n] + 3LiCl
Reattività
L'idruro di alluminio è instabile sopra i 150 °C; ha proprietà riducenti e reagisce violentemente con acqua e altre sostanze protiche liberando idrogeno.[4]
Applicazioni
L'idruro di alluminio non ha utilizzi pratici significativi, e non è disponibile in commercio. È stato studiato come possibile additivo per propellenti solidi per razzi.[5] Inoltre, essendo una sostanza contenente idrogeno nel proprio reticolo cristallino, è stato studiato come materiale di potenziale interesse nello sviluppo di veicoli alimentati a idrogeno.[6] Nessuna di queste applicazioni ha finora (2013) avuto successo.
Note
Bibliografia
- F. M. Brower, N. E. Matzek, P. F. Reigler, H. W. Rinn, C. B. Roberts, D. L. Schmidt, J. A. Snover, K. Terada, Preparation and properties of aluminum hydride, in J. Am. Chem. Soc., vol. 98, n. 9, 1976, pp. 2450–2453, DOI:10.1021/ja00425a011. URL consultato il 29 novembre 2013.
- J. Graetz, J. Reilly, G. Sandrock, J. Johnson, W. M. Zhou, J. Wegrzyn, Aluminum Hydride, AlH3, As a Hydrogen Storage Compound, in Technical Report BNL--77336-2006, 2006, DOI:10.2172/899889. URL consultato il 29 novembre 2013.
- (EN) N. N. Greenwood e A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
- O. Stecher e E. Wiberg, Über einen nichtflüchtigen, polymeren Aluminiumwasserstoff (AlH3)x und einige flüchtige Verbindungen des monomeren AlH3, in Ber. deutsch. chem. Ges., vol. 75, n. 12, 1942, pp. 2003-2012, DOI:10.1002/cber.19420751280. URL consultato il 29 novembre 2013.
- (EN) E. A. Sullivan, Hydrides, in Kirk-Othmer Encyclopedia of Chemical Technology, 4ª ed., John Wiley & Sons, 1998.
- J. W. Turley e H. W. Rinn, Crystal structure of aluminum hydride, in Inorg. Chem., vol. 8, n. 1, 1969, pp. 18–22, DOI:10.1021/ic50071a005. URL consultato il 29 novembre 2013.
Altri progetti
Altri progetti
- Wikimedia Commons
 Wikimedia Commons contiene immagini o altri file su Idruro di alluminio
Wikimedia Commons contiene immagini o altri file su Idruro di alluminio
Collegamenti esterni
- Idruro di alluminio, su webelements.com.
- Immagazzinamento dell'idrogeno, su bnl.gov. URL consultato il 22 maggio 2008 (archiviato dall'url originale il 23 agosto 2006).
V · D · M | |||||
|---|---|---|---|---|---|
| Al(I) | AlBr · AlCl · AlF · AlI · Al2O | ||||
| Al(II) | AlB2 · AlB12 · AlO | ||||
| Al(III) | AlAs · Al(BH4)3 · AlBr3 · AlCl3 · AlF3 · AlH3 · AlI3 · AlN · Al(NO3)3 · Al2(CO3)3 · Al(OH)3 · Al(OH)2OAc · Al(OH)(OAc)2 · Al(OAc)3 · Al2SO4(OAc)4 · AlP · AlPO4 · AlSb · Al(C5H7O2)3 · Al(MnO4)3 · Al2(MoO4)3 · Al2O3 · Al2S3 · Al2(SO4)3 · Al2Se3 · Al2Te3 · Al2SiO5 · Al4C3 · AlOHO · Al(OH)2CO2C17H5 · NaAlH2(OC2H4OCH3)2 · LiAlH2(OC2H4OCH3)2
| ||||
| Controllo di autorità | GND (DE) 4142120-6 |
|---|
 Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia
Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia











