Bromid vápenatý
| Bromid vápenatý | |
|---|---|
 | |
| Obecné | |
| Systematický název | Bromid vápenatý |
| Anglický název | Calcium bromide |
| Německý název | Calciumbromid |
| Sumární vzorec | CaBr2 |
| Vzhled | Bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 7789-41-5 22208-73-7 (dihydrát) 13477-28-6 (hexahydrát) |
| PubChem | 24608 |
| Číslo RTECS | EV9328000 |
| Vlastnosti | |
| Molární hmotnost | 199,89 g/mol 307,98 g/mol (hexahydrát) |
| Teplota tání | 730 °C 38,2 °C (hexahydrát) |
| Teplota varu | 810 °C |
| Teplota rozkladu | 149 °C (hexahydrát, dehydratace -6 H2O) |
| Hustota | 3,353 g/cm3 2,295 g/cm3 (hexahydrát) |
| Rozpustnost ve vodě | 125,2 g/100 g (0 °C) 132 g/100 g (10 °C) 143 g/100 g (20 °C) 153 g/100 g (25 °C) 213 g/100 g (40 °C) 278 g/100 g (60 °C) 295 g/100 g (80 °C) 312 g/100 g (105 °C) Hexahydrát 593,2 g/100 g (0 °C) 1 003,6 g/100 g (20 °C) |
| Rozpustnost v polárních rozpouštědlech | Methanol 50,4 g/100 g (0 °C) 56,2 g/100 g (20 °C) 97,8 g/100 g (60 °C) Aceton 2,72 g/100 g (20 °C) Glycerol Ethanol |
| Relativní permitivita εr | 6,15 |
| Měrná magnetická susceptibilita | −4,51·10−6 cm3g−1 −5,69×10−6 cm3g−1 (hexahydrát) |
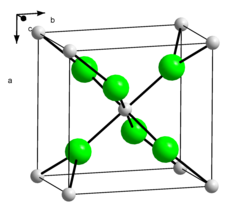
| Struktura | |
| Krystalová struktura | kosočtverečná šesterečná (hexahydrát) |
| Hrana krystalové mřížky | a= 655 pm b= 688 pm c= 434 pm Hexahydrát a= 797 pm b= 397 pm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −674,9 kJ/mol −2 500 kJ/mol (hexahydrát) |
| Entalpie rozpouštění ΔHrozp | −520,3 J/g −14,9 J/g (hexahydrát) |
| Standardní molární entropie S° | 130 JK−1mol−1 304,7 JK−1mol−1 (hexahydrát) |
| Standardní slučovací Gibbsova energie ΔGf° | −656,5 kJ/mol −2 118,9 kJ/mol (hexahydrát) |
| Bezpečnost | |
 GHS05  GHS07 Nebezpečí[1] | |
| R-věty | R36/37/38 |
| S-věty | S26, S36 |
| NFPA 704 |  0 1 0 |
Některá data mohou pocházet z datové položky. | |
Bromid vápenatý je vápenatá sůl kyseliny bromovodíkové, chemický vzorec má CaBr2. V tuhém stavu se jedná o bílé, silně hygroskopické krystalky. Je velmi dobře rozpustná ve vodě a o hodně lépe je rozpustný její hexahydrát. Dobře rozpustná je také v methanolu a poměrně málo i v acetonu.
Používá se v řezných kapalinách, léčivech, mrazicích směsích, potravinářských konzervantech, ve zpomalovačích hoření a v oblasti fotografie.[2]
CaBr2 lze připravit například reakcí oxidu vápenatého s kyselinou bromovodíkovou nebo reakcí kovového vápníku s elementárním bromem.
Při silném zahřívání CaBr2 na vzduchu vzniká oxid vápenatý a brom:
- 2 CaBr2 + O2 → 2 CaO + 2 Br2
V této reakci dochází k oxidaci bromidu na brom.
Reference
V tomto článku byl použit překlad textu z článku Calcium bromide na anglické Wikipedii.
- ↑ a b Calcium bromide. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Chemical Land 21 [online]. [cit. 2008-12-25]. Dostupné online. Je zde použita šablona
{{Cite web}}označená jako k „pouze dočasnému použití“.
Externí odkazy
- MSDS - Calcium bromide hydrate Archivováno 4. 3. 2016 na Wayback Machine.
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
| Bromidy s prvkem v oxidačním čísle II. | |
|---|---|
| Bromid americiumnatý (AmBr2) • Bromid barnatý (BaBr2) • Bromid berylnatý (BeBr2) • Bromid vápenatý (CaBr2) • Bromid kademnatý (CdBr2) • Bromid kalifornatý (CfBr2) • Bromid kobaltnatý (CoBr2) • Bromid chromnatý (CrBr2) • Bromid měďnatý (CuBr2) • Bromid europnatý (EuBr2) • Bromid železnatý (FeBr2) • Bromid germanatý (GeBr2) • Bromid rtuťnatý (HgBr2) • Bromid hořečnatý (MgBr2) • Bromid manganatý (MnBr2) • Bromid molybdenatý (MoBr2) • Bromid nikelnatý (NiBr2) • Bromid olovnatý (PbBr2) • Bromid palladnatý (PdBr2) • Bromid platnatý (PtBr2) • Bromid radnatý (RaBr2) • Bromid ruthenatý (RuBr2) • Bromid sirnatý (SBr2) • Bromid selenatý (SeBr2) • Bromid tellurnatý (TeBr2) • Bromid polonatý (PoBr2) • Bromid samarnatý (SmBr2) • Bromid strontnatý (SrBr2) • Bromid cínatý (SnBr2) • Bromid titanatý (TiBr2) • Bromid vanadnatý (VBr2) • Bromid wolframnatý (WBr2) • Bromid ytterbnatý (YbBr2) • Bromid zinečnatý (ZnBr2) | |
| Anorganické soli vápenaté | |
|---|---|
| Halogenidy a pseudohalogenidy | Fluorid vápenatý (CaF2) • Bromid vápenatý (CaBr2) • Chlorid vápenatý (CaCl2) • Jodid vápenatý (CaI2) • Kyanid vápenatý (Ca(CN)2) • Kyanamid vápenatý (CaNCN) • Thiokyanatan vápenatý (Ca(SCN)2) |
| Soli kyslíkatých kyselin (neuvedeny soli | Chlornan vápenatý (Ca(OCl)2) • Chlorečnan vápenatý (Ca(ClO3)2) • Chloristan vápenatý (Ca(ClO4)2) • Bromičnan vápenatý (Ca(BrO3)2) • Jodičnan vápenatý (Ca(IO3)2) • Jodistan vápenatý (Ca(IO4)2) • Siřičitan vápenatý (CaSO3) • Hydrogensiřičitan vápenatý (Ca(HSO3)2) • Síran vápenatý (CaSO4) • Selenan vápenatý (CaSeO4) • Telluričitan vápenatý (CaTeO3) • Teluran vápenatý (CaTeO4) • Dusitan vápenatý (Ca(NO2)2) • Dusičnan vápenatý (Ca(NO3)2) • Fosfornan vápenatý (Ca(PO2H2)2) • Hydrogenfosforitan vápenatý (CaHPO3) • Dihydrogenfosforečnan vápenatý (Ca(H2PO4)2) • Hydrogenfosforečnan vápenatý (CaHPO4) • Fosforečnan vápenatý (Ca3(PO4)2) • Difosforečnan vápenatý (Ca2P2O7) • Arsenitan vápenatý (Ca(AsO2)2) • Arseničnan vápenatý (Ca3(AsO4)2) • Hydrogenuhličitan vápenatý (Ca(HCO3)2) • Uhličitan vápenatý (CaCO3) • Šťavelan vápenatý (Ca(CO2)2) • Křemičitan vápenatý (Ca2SiO4) • Boritan vápenatý (Ca3(BO3)2) • Manganistan vápenatý (Ca(MnO4)2) • Chroman vápenatý (CaCrO4) • Dichroman vápenatý (CaCr2O7) • Molybdenan vápenatý (CaMoO4) • Wolframan vápenatý (CaWO4]) • Vanadičnan vápenatý (Ca(VO3)2) • Titaničitan vápenatý (CaTiO3) • Hlinitan monovápenatý (CaAl2O4) • Heptahlinitan dodekavápenatý |
| Soli tvořené záměnou vodíku ze sloučenin typu prvekx – vodíky | Hydrid vápenatý (CaH2) • Hydroxid vápenatý (Ca(OH)2) • Oxid vápenatý (CaO) • Peroxid vápenatý (CaO2) • Hydrogensulfid vápenatý (Ca(SH)2) • Sulfid vápenatý (CaS) • Polysulfid vápenatý (CaSn) • Polonid vápenatý (CaPo) • Amid vápenatý (Ca(NH2)2) • Imid vápenatý (CaNH) • Nitrid vápenatý (Ca3N2) • Azid vápenatý (Ca(N3)2) • Fosfid vápenatý (Ca3P2) |
| Jiné | Thiosíran vápenatý (CaS2O3) • Karbid vápenatý (CaC2) • Hexaborid vápenatý (CaB6) • Monofosfid vápenatý (Ca2P2) • Disilicid vápenatý (CaSi2) |








